酸性環境における腫瘍の悪性化に
コレステロール代謝制御タンパク質が寄与することを発見
- プレスリリース
2017年3月1日
- 大澤 毅
- (東京大学先端科学技術研究センター システム生物医学分野 特任助教)
- 近藤 彩乃
- (東京大学先端科学技術研究センター ゲノムサイエンス分野 博士課程学生:当時)
- 油谷 浩幸
- (東京大学先端科学技術研究センター ゲノムサイエンス分野 教授)
- 酸性環境の腫瘍組織において、コレステロール代謝を制御するタンパク質が活性化し、種々の代謝酵素の発現を変化させることで、腫瘍増殖および患者予後に関与することを明らかにしました。
- これまで未知であった、酸性環境におけるシグナル伝達やがん細胞の応答メカニズムを明らかにしました。
- 酸性環境におけるがん細胞の転写・代謝応答を標的とした新規創薬の開発に繋がることが期待されます。
3.発表概要:
固形がんにおいては不完全な血管構築による血流不全から、がんの中心部が低酸素状態に陥りやすく、その結果として酸性状態(アシドーシス、注1)になることが知られています。しかし、酸性状態におけるがん細胞の応答メカニズムや酸性環境によるがん悪性化への影響は、これまで明らかにされていませんでした。東京大学先端科学技術研究センターの大澤毅特任助教、近藤彩乃博士課程学生(当時)、油谷浩幸教授らの研究グループは、酸性状態のがん組織において、コレステロール代謝のマスターレギュレーター(注2)である転写因子「SREBP2(注3)」が活性化され、コレステロール合成経路や酢酸代謝経路における一連の酵素群の発現を促進し、腫瘍増殖および患者予後に関与するなどがんの悪性化に寄与することを明らかにしました。本研究成果は、2017年2月28日12時(米国東部標準時間)に電子ジャーナル「Cell Reports」に掲載されました。
本研究は、国立研究開発法人新エネルギー・産業技術総合開発機構(NEDO)「後天的ゲノム修飾のメカニズムを活用した創薬基盤技術開発」の研究成果をシーズとし、国立研究開発法人日本医療研究開発機構(AMED)「次世代がん医療創生研究事業(P-CREATE)」や科学研究費補助金の支援を得て行われました。
4.発表内容:
固形がんにおいては不完全な血管構築による血流不全から、がんの中心部が低酸素状態に陥りやすく、その結果として解糖系代謝(注4)が亢進し酸性状態になる事が知られています。しかし、酸性状態におけるがん細胞の応答メカニズムや酸性環境によるがん悪性化への影響は、これまで明らかになっていませんでした。本研究グループは、酸性環境における転写制御因子を予測するために、酸性状態を模した培養系を用い、がん細胞に対しトランスクリプトーム(注5)および、エピゲノム(注6)の網羅的オミクス統合解析(注7)を行いました。その結果、これまでがんにおいてどのような役割を果たしているか不明であった転写因子SREBP2が、酸性環境で活性化している可能性を見出しました。さらに研究グループは、培養細胞とマウスを用いた解析から、SREBP2が確かに酸性環境で核内移行して活性化すること、結果としてコレステロールや酢酸を代謝する酵素群の発現を上昇させ、腫瘍増殖および患者予後に関与することを明らかにしました(図1)。
近年、がん細胞の生存や悪性化メカニズムとして、低酸素や低栄養等の周辺環境に応じたトランスクリプトーム、エピゲノム変化や代謝適応が注目されています。本研究にて得られた知見は、低酸素や低栄養だけでなく酸性という環境が、これまでがんでの機能が明らかにされていなかったSREBP2という転写因子を介してトランスクリプトーム、エピゲノムや代謝を変化させ、がん増殖や悪性化に関わることを初めて示唆するもので、酸性環境におけるがん細胞の転写・代謝応答に着目した新規創薬の開発に繋がることが期待されます。
5.発表雑誌:
雑誌名:「Cell Reports」
論文タイトル:Extracellular acidic pH activates the Sterol regulatory element-binding protein 2 to promote tumor progression
著者:Ayano Kondo, Shogo Yamamoto, Ryo Nakaki, Teppei Shimamura, Takao Hamakubo, Juro Sakai, Tatsuhiko Kodama, Tetsuo Yoshida, Hiroyuki Aburatani, and Tsuyoshi Osawa
6.問い合わせ先:
<研究について>
東京大学先端科学技術研究センター システム生物医学分野
特任助教 大澤 毅(おおさわ つよし)
<AMED事業について>
国立研究開発法人日本医療研究開発機構(AMED)
戦略推進部 がん研究課
〒100-0004 東京都千代田区大手町一丁目7番1号
TEL:03-6870-2221
E-mail:cancer@amed.go.jp
7.用語解説:
(注1)酸性状態(アシドーシス):
がん組織内で正に帯電したプロトンや乳酸が蓄積することによりpHが低下すること。
(注2)マスターレギュレーター:
形質発現などを担う一群の機能的に関連した遺伝子群を制御する、主要転写制御因子。
(注3)SREBP2:
コレステロール合成を制御する転写因子。コレステロール生合成経路酵素群の転写を亢進し酵素群の発現を上昇させる。
(注4)解糖系代謝:
グルコースを燃料とし、ミトコンドリア電子伝達系を介さずにエネルギーを産生する経路。増殖の速いがん細胞で亢進することが知られており、プロトンや乳酸を産生するため、結果的にがん組織の内部が酸性状態に陥る。
(注5)トランスクリプトーム:
特定の状況下での細胞内の全転写産物(全RNA)のこと。細胞内の全DNAの塩基配列情報であるゲノムは原則として同一個体内のすべての細胞で同一だが、トランスクリプトームは各細胞や条件で異なる。
(注6)エピゲノム:
DNAのメチル化とヒストン修飾で維持・伝達される、後天的に書き換えられる遺伝情報。エピゲノムの変化が、トランスクリプトームの変化を引き起こすことが知られている。
(注7)オミクス統合解析:
生体内の分子群(DNAやRNA、タンパク質、代謝物、脂質等)を網羅的に解析することで生命現象を包括的に調べる手法を『オミクス解析』と呼ぶ。このオミクス解析から得られた多階層の情報を統合して解析する方法。
8. 添付資料:
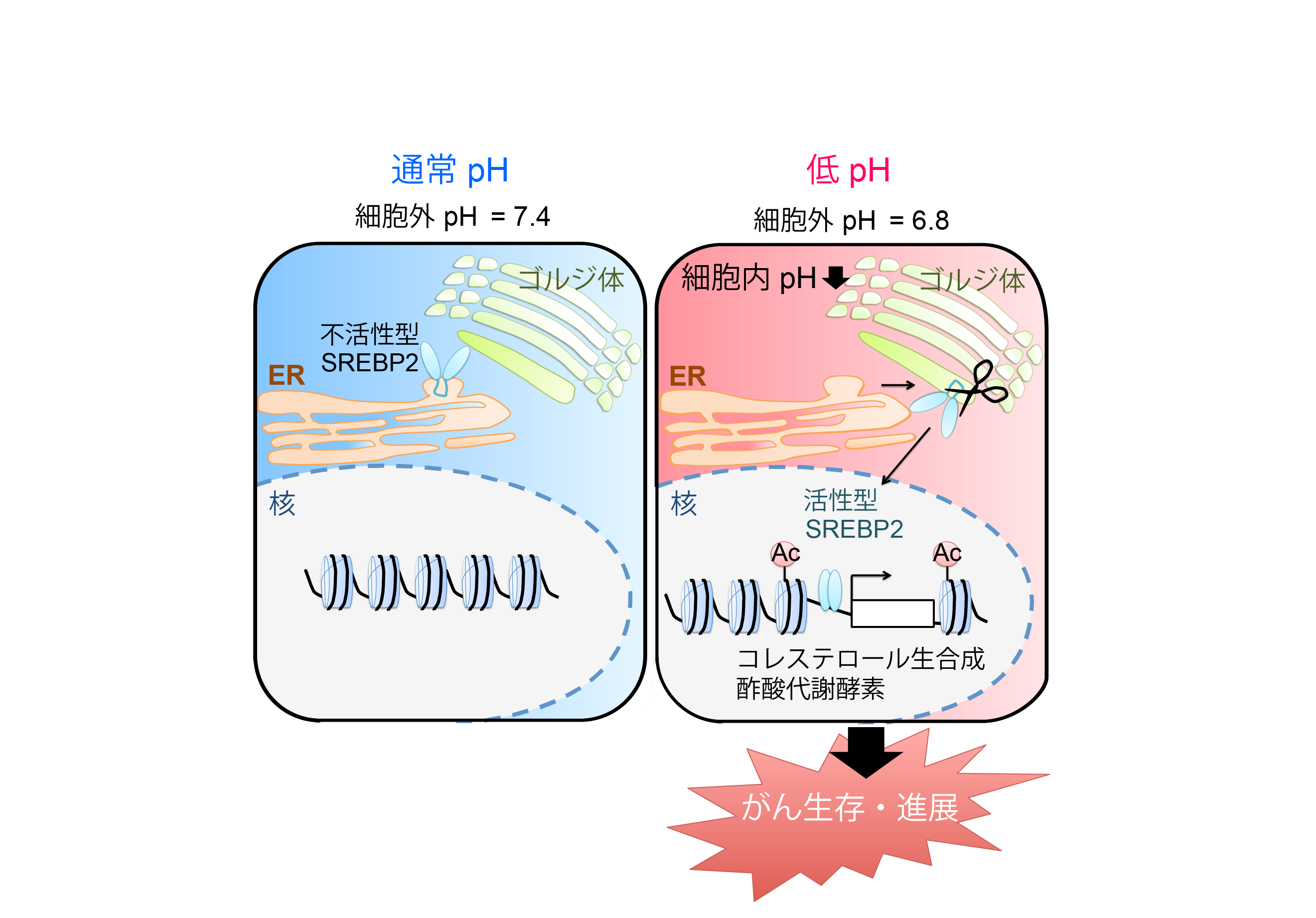
図1:酸性環境におけるがん細胞の応答メカニズム。
(左)細胞外pH 7.4の通常状態では、SREBP2はERに局在し不活性型である。
(右)一方、細胞外pH 6.8の酸性状態にがん細胞が陥ると、細胞内のpHが低下し、SREBP2がゴルジ体を経由して核内に移行し活性化する。結果として、コレステロール生合成や酢酸代謝に関連する酵素群の発現を誘導することで、がんの生存や進展に寄与する。
関連タグ

