冠動脈疾患発症に関する遺伝的変異の影響を解明
-60万人超の大規模ゲノム解析で明らかに-
- プレスリリース
2020年10月6日
理化学研究所
東京大学
日本医療研究開発機構
理化学研究所(理研)生命医科学研究センター循環器ゲノミクス・インフォマティクス研究チームの伊藤薫チームリーダー、小山智史特別研究員、久保充明副センター長(研究当時)、東京大学の小室一成教授、鎌谷洋一郎教授、油谷浩幸教授、村上善則教授、野村征太郎特任助教らの国際共同研究グループ※は、京都大学ゲノム医学センター[1]、JPHC研究[2]、J-MICC研究[3]、OACIS研究[4]と共同で、日本人約17万人のゲノムデータに加え、約5,000人の全ゲノムシークエンスデータを応用し冠動脈疾患を対象としたゲノム解析を行いました。さらにヨーロッパ人集団との統合解析により、冠動脈疾患に関わる疾患感受性座位[5]を新たに同定し、日本人における冠動脈疾患の発症リスクを予測する遺伝的リスクスコア(GRS)[6]を作成しました。
本研究成果は、冠動脈疾患の発症に関わる分子機構の詳しい理解に役立つだけでなく、遺伝情報に基づいた予防・治療の個別化に貢献すると期待できます。
今回、国際共同研究グループは、バイオバンク・ジャパン[7]のゲノムデータを用いて、日本人約17万人のゲノムワイド関連解析(GWAS)[8]を行い、これまでのヨーロッパ人集団を対象とした研究では同定されていなかった8領域を含む、48の冠動脈疾患に関わる疾患感受性座位を同定しました。さらに、過去に行われたヨーロッパ人集団でのGWASの結果と統合し、計60万人を超える大規模な民族横断解析を行った結果、新たに同定された35領域を含む175の疾患感受性座位を同定しました。これまでヨーロッパ人集団のGWASの結果はGRSの作成において日本人をはじめとする非ヨーロッパ人集団への応用が難しいと考えられていましたが、本研究ではヨーロッパ人集団のデータに日本人のデータを加えることによって、高い予測性能を示すGRSの作成に成功しました。
本研究は、科学雑誌『Nature Genetics』の掲載に先立ち、オンライン版(10月5日付:日本時間10月6日)に掲載されました。
研究支援
本研究は、日本医療研究開発機構(AMED)のオーダーメイド医療の実現プログラム「疾患関連遺伝子等の探索を効率化するための遺伝子多型情報の高度化(研究開発代表者:久保充明)」、ゲノム医療実現推進プラットフォーム事業「マルチオミックス連関による循環器疾患における次世代型精密医療の実現(研究開発代表者:小室一成)」の支援を受けて行われました。
1.背景
冠動脈疾患とは、心筋梗塞、狭心症など、心臓に栄養を送る冠動脈に狭窄や閉塞を来す疾患の総称であり、その背景には高血圧・脂質異常症など、動脈硬化を進行させる病態が存在します。冠動脈疾患は世界の死因の第一位を占めることから、原因を理解し、有効な予防・治療方法を確立することが求められています。
冠動脈疾患は遺伝性[9]が高い疾患であり、これまでに多くの研究が行われ、遺伝的変異と冠動脈疾患との関連が多数報告されてきました。冠動脈疾患との強い関連が示されたPCSK9遺伝子については、それをターゲットとした治療薬の開発に成功しています。また最近では、遺伝情報だけから作成される「遺伝的リスクスコア(GRS)」が、疾患発症を高い精度で予測することが明らかになってきました。
このように、遺伝情報に基づいて病気の成り立ちを理解すること、治療薬を開発すること、病気の発症リスクを予測することは、今後、冠動脈疾患の医学・医療を進歩させるために重要な役割を果たすと期待されています。しかし、これまでの研究はヨーロッパ人集団を主な対象としており、それらの研究成果が日本人を含む東アジア人集団にも適応可能かどうかについては明らかではありませんでした。また、遺伝的変異の分布には民族差が大きいことが知られていますが、ヨーロッパ人集団にはない遺伝的変異と冠動脈疾患との関連については、これまで十分に研究されていませんでした。
今後、日本において遺伝情報に基づいた冠動脈疾患の医療を展開するにあたり、日本人を対象にしたデータの作成は重要な課題です。そこで、国際共同研究グループは、バイオバンク・ジャパンに登録されている約17万人の被験者を対象に、冠動脈疾患の発症に関わる遺伝的変異を探索しました。
2.研究手法と成果
国際共同研究グループは、バイオバンク・ジャパンに登録されている約25,892人の冠動脈疾患患者と142,336人の対照群、合わせて約17万人のゲノム配列を比較し、冠動脈疾患の患者に特徴的に見られる遺伝的変異を網羅的に検出するゲノムワイド関連解析(GWAS)を行いました。本研究は、非ヨーロッパ人集団を対象とした冠動脈疾患に関するGWASとしては、世界最大規模のプロジェクトです。
GWASの実施に先立ち、まず、4,417人の日本人の全ゲノムシークエンス[10]のデータを用いて、遺伝型インピュテーション[11]のためのリファレンスパネル[12]を新しく開発しました。このリファレンスパネルは、日本人に特異的なレアバリアント[13]を多く含み、民族集団が一致していることから、これまでの約2倍の遺伝的変異について推定することができました。
この高密度に推定された遺伝情報を用いて、GWASを行った結果、ゲノム全体にわたる48の冠動脈疾患に関わる疾患感受性座位と73の遺伝的変異を同定しました。48の疾患感受性座位のうち8領域は、これまでのヨーロッパ人集団を対象とした研究では同定されていませんでした。17番染色体に存在するRNF213遺伝子のミスセンス変異[14]は、これまで小児で見られるもやもや病[15]の原因遺伝子の変異として知られていました。日本での先行研究で冠動脈疾患との関連が報告されていました注)が、今回の研究によってGWASの枠組みとしては初めて冠動脈疾患との関連が示されました。この理由には、このミスセンス変異がヨーロッパ人集団には存在せず、これまでのヨーロッパ人集団を対象としたGWASでは評価できなかったことが挙げられます。
通常、GWASで発見される疾患に関連する遺伝的変異のオッズ比は1.1-1.2と小さなものがほとんどです。原因としてこれまでのGWASでは集団内頻度1%以下の遺伝的変異の病原性を精密に推定できなかったことが挙げられます。今回の研究では日本人に特化したリファレンスパネルを使用したため、低頻度(集団内頻度1%以下)から超低頻度変異(集団内頻度0.1%以下)の病原性を精密に推定することができました。病原性に最も強く影響したのは、コレステロール代謝に重要なLDL受容体の働きを大幅に低下させる遺伝的変異(ストップゲイン変異[14]、LDLR p.K811X、集団内頻度 0.038%)でした。この変異は、冠動脈疾患を発症するリスク(オッズ比[16])が5と強い影響を示しました(図1)。この変異を持つと、持たない人に比べ冠動脈疾患を発症する可能性が5倍になると解釈できます。また、この変異を持つと血清総コレステロール値が平均57mg/dL上昇することも分かりました。
一方で、冠動脈疾患に保護的な変異も検出されました。PCSK9遺伝子は、LDL受容体の働きを阻害して冠動脈疾患の発症を促進することが知られています。PCSK9遺伝子の働きを低下させる遺伝的変異(ミスセンス変異、PCSK9 p.R93C)を持つと、血清総コレステロール値が平均20mg/dL低下し、オッズ比が0.6に低下することが示されました(図1)。さらに、これらの変異は日本人特有のものであり、他の民族集団には見られないことも分かりました。
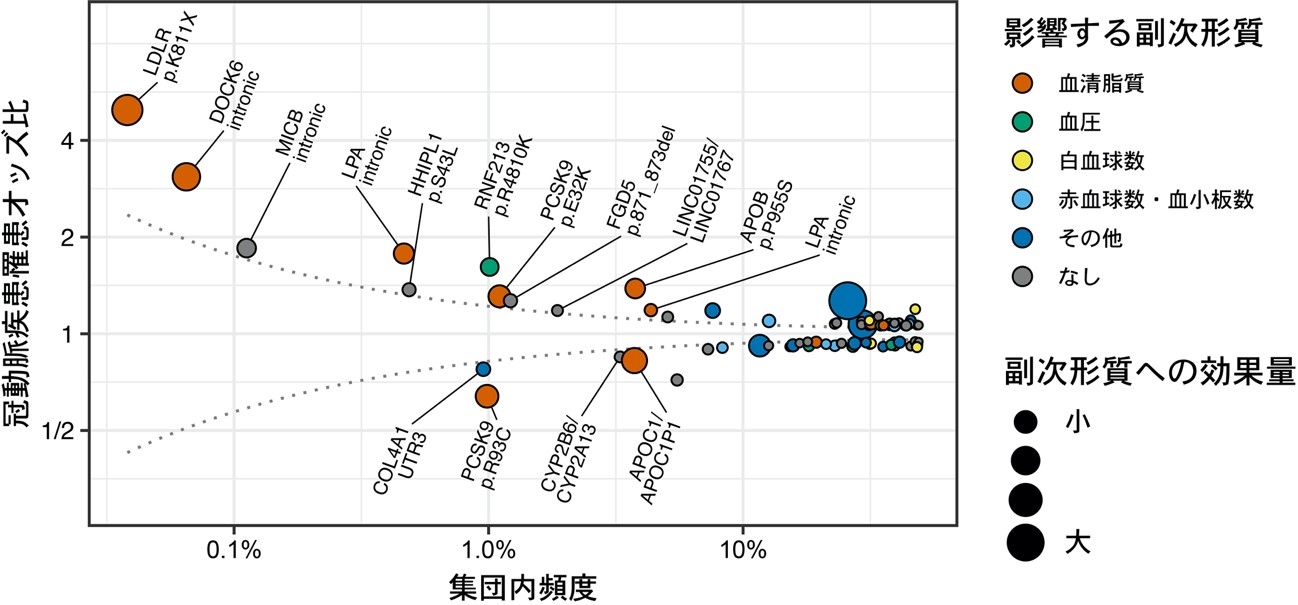
横軸は集団内頻度を、縦軸は冠動脈疾患罹患オッズ比を示す。各点の色は、それぞれの変異が関連を示した副次形質を示している。赤は、血清脂質測定値(コレステロール値・中性脂肪値)との関連を示す。多くの変異が血清脂質との関連を示しているが、特にLDLR p.K811Xはオッズ比5で冠動脈疾患発症のリスクが高く、反対にPCSK9 p.R93Cはオッズ比0.6で発症リスクが低いことが分かった。
次に、日本人のGWASの結果(約17万人)をヨーロッパ人集団のGWASの結果(CARDIoGRAMplusC4D研究[17]の約18万人 、UKバイオバンク[18]の約30万人)と統合し、計60万人を超える世界最大規模の冠動脈疾患における民族横断的GWASを行いました。その結果、冠動脈疾患と関連を示す175の疾患感受性座位を同定しました。このうち35領域は新たに同定されたもので、その中には冠動脈疾患における最も重要な治療薬であるスタチン系脂質異常治療薬のターゲットであるHMGCR遺伝子が含まれていました。このように今回見つかった疾患感受性座位の中には、冠動脈疾患の治療薬のターゲットとして有用な遺伝子が含まれている可能性があり、今後の治療薬開発において重要な情報になると考えられます。
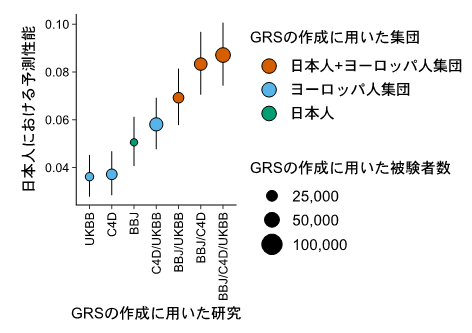
続いて、今回得られた遺伝的変異と疾患の関連解析結果を用いてGRSを作成し、その予測性能を日本のゲノムコホート(JPHC研究、J-MICC研究、OACIS研究)で調べました。特定の民族集団のGWASの結果から算出したGRSは他民族集団には適合せず、予測性能が低いことは以前から知られていました。本研究においてもヨーロッパ人集団のGWAS結果から作成したGRSは、日本人のGWAS結果から作成したGRSと比較して、日本人における予測性能が低いことが確認されました。そこで、民族横断的GWASの結果を用いてGRSを作成したところ、民族横断的GRSの性能は、日本人データによるGRSやヨーロッパ人集団データによるGRSを上回ることが分かりました(図2)。
GWASはこれまでヨーロッパ人集団を対象に多く行われてきたため、ヨーロッパ人集団のデータは豊富に蓄積されていますが、アジア人を含む非ヨーロッパ人集団のデータは少なく、非ヨーロッパ人集団ではGRSによるリスク予測の恩恵を受けにくいという点が問題視されていました。今回の結果は、今後非ヨーロッパ人集団におけるGRSを作成するにあたって、既存データの統合が有効であることを示しています。
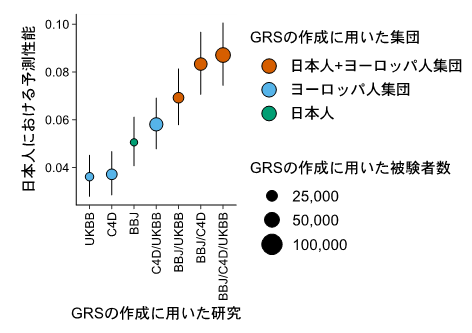
縦軸は、それぞれのGRSによる日本人における冠動脈疾患の発症予測性能を示す。各点の色は、それぞれのGRS作成に用いたデータに含まれる集団を、各点の大きさは、データに含まれる被験者数を表している。日本人のデータを含むGRS(赤・緑)は、被験者数が少ないにもかかわらず良い予測成績を示している。
注)Morimoto, T. et al. Significant association of RNF213 p.R4810K, a moyamoya susceptibility variant, with coronary artery disease. PLoS ONE 12(4): e0175649. 2017.
3.今後の期待
本研究において新たに同定された疾患感受性座位は、今後の冠動脈疾患の病態の理解、治療薬の発見において重要な情報を提供すると考えられます。また、日本人向けに最適化された冠動脈疾患のGRSは、今後の遺伝情報に基づく精密医療の実現において有効に活用されると期待できます。
本研究の成果は、ナショナルバイオサイエンスデータベースセンター[19]を介して公開しており(https://humandbs.biosciencedbc.jp/hum0014-v20) 、研究目的であれば自由に利用できます。
、研究目的であれば自由に利用できます。
4.論文情報
<タイトル>
Population-specific and trans-ancestry genome-wide analyses identify distinct and shared genetic risk loci for coronary artery disease
<著者名>
Satoshi Koyama, Kaoru Ito, Chikashi Terao, Masato Akiyama, Momoko Horikoshi, Yukihide Momozawa, Hiroshi Matsunaga, Hirotaka Ieki, Kouichi Ozaki, Yoshihiro Onouchi, Atsushi Takahashi, Seitaro Nomura, Hiroyuki Morita, Hiroshi Akazawa, Changhoon Kim, Jeong-sun Seo, Koichiro Higasa, Motoki Iwasaki, Taiki Yamaji, Norie Sawada, Shoichiro Tsugane, Teruhide Koyama, Hiroaki Ikezaki, Naoyuki Takashima, Keitaro Tanaka,Kokichi Arisawa, Kiyonori Kuriki, Mariko Naito, Kenji Wakai, Shinichiro Suna, Yasuhiko Sakata, Hiroshi Sato, Masatsugu Hori, Yasushi Sakata, Koichi Matsuda, Yoshinori Murakami, Hiroyuki Aburatani, Michiaki Kubo, Fumihiko Matsuda, Yoichiro Kamatani, and Issei Komuro
<雑誌>
Nature Genetics
<DOI>
10.1038/s41588-020-0705-3
5.補足説明
[1] 京都大学ゲノム医学センター
本研究では、京都大学大学院医学研究科附属ゲノム医学センターと理化学研究所と共同で作成した全ゲノムシークエンスデータが、共同研究として使用された。同データは難病プラットフォーム(https://www.raddarj.org) において、難病研究コントロールとしても利用されている。京都大学ゲノム医学センターでは次世代の疾患解析モデルの構築を目指している。
において、難病研究コントロールとしても利用されている。京都大学ゲノム医学センターでは次世代の疾患解析モデルの構築を目指している。
[2] JPHC研究
がんや脳卒中、心筋梗塞、糖尿病といった生活習慣病における予防要因や危険要因を明らかにし、日本人の生活習慣病の予防と健康寿命の延伸に役立てることを目的としたコホート研究。全国11の保健所と国立がん研究センター、国立循環器研究センター、大学、研究期間、医療機関が共同で実施している。JPHCはJapan Public Health Center-based Prospective Studyの略。詳細は国立がん研究センター 社会と健康研究センター 予防研究グループ 多目的コホート研究のページ(https://epi.ncc.go.jp/jphc) を参照。
を参照。
[3] J-MICC研究
がんやその他の生活習慣病に対し、遺伝要因や環境要因、生態指標と疾患リスクとの関係を測定し、予防対策に必要な基礎データを築くことを目的とした大規模追跡調査。13の大学・がんセンターが共同して実施している。2005年に開始し、千葉県から沖縄県におよぶ地域で10万人以上が参加し、20年間の追跡を計画している。J-MICCはJapan Multi-Institutional Collaborative Cohort Studyの略。詳細は日本多施設共同コーホート研究のウェブサイト(http://www.jmicc.com) を参照。
を参照。
[4] OACIS研究
阪神地区の25の医療施設において急性心筋梗塞患者を対象とし、遺伝子や臨床背景、治療経過、予後などの情報収集・解析を行い、心筋梗塞の病態を理解し、治療の改善につなげることを目的としたプロジェクト。大阪大学が中心となって構築された。OACISはOsaka Acute Coronary Insufficiency Studyの略。
[5] 疾患感受性座位
単一遺伝子病の原因遺伝子のように、遺伝子に変異があると必ず発症するというものではなく、変異があると発症しやすくなったり、逆に発症しにくくなったりするような染色体上の領域のこと。
[6] 遺伝的リスクスコア(GRS)
ゲノム上の数万から数百万の遺伝的変異の影響を足し合わせることで計算される、個人の疾患へのかかりやすさの推定値や身長・体重の予測値のこと。冠動脈疾患であれば、この値が高いほど発症の可能性が高いとされる。GRSはGenetic Risk Scoreの略。
[7] バイオバンク・ジャパン
2003年に開始されたオーダーメイド医療実現化プロジェクトの基盤事業であり、東京大学医科学研究所内に設置されている。今回の研究で使用した第一期コホートでは、日本人約20万人から収集したDNAや血清試料を臨床情報・ゲノム情報とともに厳重に保管しており、研究者へ試料や情報を提供している。詳細はバイオバンク・ジャパンのウェブサイト(https://biobankjp.org/index.html) を参照。
を参照。
[8] ゲノムワイド関連解析(GWAS)
疾患の発症に影響がある遺伝的変異を網羅的に検出する方法。疾患の罹患状態と全ての遺伝的変異の関係について統計解析を行い、厳格な水準を満たした遺伝的変異だけが疾患に関連する変異として報告される。2002年に理化学研究所が世界に先駆けて報告した手法。GWASはGenome Wide Association Studyの略。
[9] 遺伝性
ある病気が血縁者内に多く見られる場合、「遺伝性が高い」という。糖尿病や冠動脈疾患は、比較的遺伝性の高い一般複合性疾患として知られる。
[10] 全ゲノムシークエンス
ゲノム上の遺伝的変異を網羅的に検出する方法。以前は1人のゲノムの全ゲノムをシークエンスするためには国家プロジェクト規模の予算を必要としていたが、技術の進歩によって現在では大規模に実施できるようになった。
[11] 遺伝型インピュテーション
全ゲノムシークエンスの結果を用いて、一般的に用いられているマイクロアレイによる遺伝的変異解析では検出されない遺伝的変異を推定する方法。遺伝的解析に使用できる変異数を増大させることができる。
[12] リファレンスパネル
遺伝型インピュテーションに用いるための全ゲノムシークエンスデータのこと。これまでは1000ゲノムプロジェクトなどで作成されたデータを用いることが多かったが、全ゲノムシークエンスの一般化により、民族・疾患特異的なリファレンスパネルが使用可能になりつつある。
[13] レアバリアント
集団内での頻度が1%以下である遺伝的変異をさす。効果の強い変異は集団内に広まりにくいため、病的意義の強い変異は頻度が低い傾向にある。
[14] ミスセンス変異、ストップゲイン変異
タンパク質に翻訳されるゲノム領域で、タンパク質への翻訳を止めてしまう変異を「ストップゲイン変異」という。この変異があると、本来得られるタンパク質よりも短いものが生成されるため、その機能に与える影響が非常に大きい。「ミスセンス変異」はタンパク質に翻訳の際にアミノ酸の置換が起きるが、一部分の置換に留まるため、タンパク質部位や置換の内容によってその影響はさまざまである。
[15] もやもや病
日本で初めて発見された疾患で、脳血管中のウィリス動脈輪が進行性に閉塞するために側副結構路が発達する。小児の脳卒中の原因として代表的なものである。
[16] オッズ比
発症リスクの大きさの指標。基準とするものに対して、発症するリスクが何倍に上がるかを表す。
[17] CARDIoGRAMplusC4D研究
冠動脈疾患に関する世界最大のゲノム研究。米国の研究者らが主導し、多くのゲノムコホートを統合して解析を行なっている。冠動脈疾患のゲノム研究における多くの発見は、この研究に根ざしている。CARDIoGRAMplusC4Dは、Coronary ARtery DIsease Genome wide Replication and Meta-analysis (CARDIoGRAM) plus The Coronary Artery Disease (C4D) Geneticsの略。
[18] UKバイオバンク
英国において設立、維持されている50万人規模のゲノムバイオバンクであり、参加者のゲノム情報、医療情報などを収集している。研究者が申請すれば、個人情報の保護の範囲内で自由にゲノム研究を行うことができる。
[19] ナショナルバイオサイエンスデータベースセンター(NBDC)
国内の生命科学研究から生み出されたビッグデータを収集し、共有・整理・統合するためのナショナルデータベース。バイオバンク・ジャパンの研究成果は、NBDCを通じて入手・利用できる。詳細はNBDCのウェブサイト(https://biosciencedbc.jp/) を参照。
を参照。
6.発表者・機関窓口
<発表者>
- 理化学研究所
- 生命医科学研究センター 循環器ゲノミクス・インフォマティクス研究チーム
- チームリーダー
- 伊藤 薫(いとう かおる)
- 特別研究員
- 小山 智史(こやま さとし)
- 統合生命医科学研究センター(研究当時)
- 副センター長(研究当時)
- 久保 充明(くぼ みちあき)
- 東京大学医学部附属病院 循環器内科
- 教授
- 小室 一成(こむろ いっせい)
- 特任助教
- 野村 征太郎(のむら せいたろう)
- 東京大学大学院新領域創成科学研究科
- メディカル情報生命専攻 複雑形質ゲノム解析分野
- 教授
- 鎌谷 洋一郎(かまたに よういちろう)
- (理研 生命医科学研究センター ゲノム解析応用研究チーム 客員主管研究員)
- 東京大学先端科学技術研究センター ゲノムサイエンス分野
- 教授
- 油谷 浩幸(あぶらたに ひろゆき)
- 東京大学医科学研究所 人癌病因遺伝子分野
- 教授
- 村上 善則(むらかみ よしのり)
- 理化学研究所
- 生命医科学研究センター
- 循環器ゲノミクス・インフォマティクス研究チーム
- チームリーダー
- 伊藤 薫(いとう かおる)
- 特別研究員
- 小山 智史(こやま さとし)
- 研修生
- 松永 紘(まつなが ひろし)
- (東京大学大学院医学系研究科 循環器内科学 大学院生)
- 研修生
- 家城 博隆(いえき ひろたか)
- (東京大学大学院医学系研究科 循環器内科学 大学院生)
- 客員研究員
- 尾崎 浩一(おざき こういち)
- (国立長寿医療研究センター メディカルゲノムセンター臨床ゲノム解析推進部 部長)
- 客員研究員
- 尾内 善広(おのうち よしひろ)
- (千葉大学大学院 医学研究院 公衆衛生学 教授)
- ゲノム解析応用研究チーム
- チームリーダー
- 寺尾 知可史(てらお ちかし)
- 客員研究員
- 秋山 雅人(あきやま まさと)
- (九州大学大学院 医学研究院 講師)
- 糖尿病・代謝ゲノム疾患研究チーム
- チームリーダー
- 堀越 桃子(ほりこし ももこ)
- 基盤技術開発研究チーム
- チームリーダー
- 桃沢 幸秀(ももざわ ゆきひで)
- 統合生命医科学研究センター (研究当時)
- 副センター長(研究当時)
- 久保 充明(くぼ みちあき)
- 東京大学大学院医学系研究科 循環器内科学(東京大学医学部附属病院 循環器内科)
- 教授
- 小室 一成(こむろ いっせい)
- 講師
- 森田 啓行(もりた ひろゆき)
- 講師
- 赤澤 宏(あかざわ ひろし)
- 特任助教
- 野村 征太郎(のむら せいたろう)
- 東京大学先端科学技術研究センター ゲノムサイエンス分野
- 教授
- 油谷 浩幸(あぶらたに ひろゆき)
- 東京大学大学院新領域創成科学研究科
- メディカル情報生命専攻 複雑形質ゲノム解析分野
- 教授
- 鎌谷 洋一郎(かまたに よういちろう)
- (理研 生命医科学研究センター ゲノム解析応用研究チーム 客員主管研究員)
- メディカル情報生命専攻 クリニカルシークエンス分野
- 教授
- 松田 浩一(まつだ こういち)
- 東京大学医科学研究所 人癌病因遺伝子分野
- 教授
- 村上 善則(むらかみ よしのり)
- 京都大学大学院医学研究科 附属ゲノム医学センター
- 教授
- 松田 文彦(まつだ ふみひこ)
- 関西医科大学 附属生命医学研究所ゲノム解析部門
- 教授
- 日笠 幸一郎(ひがさ こういちろう)
- Bioinformatics Institute Macrogen Inc.
- チャンフン・キム(Changhoon Kim)
- Seoul National University Bundang Hospital
- Professor
- チョンソン・ソ(Jeong-sun Seo)
- 国立循環器病研究センター研究所 病態ゲノム医学部
- 部長
- 高橋 篤(たかはし あつし)
- 国立がん研究センター
- 社会と健康研究センター
- センター長
- 津金 昌一郎(つがね しょういちろう)
- 疫学・予防研究グループ 疫学研究部
- 部長
- 岩崎 基(いわさき もとき)
- 室長
- 山地 樹(やまじ たいき)
- 室長
- 澤田 典絵(さわだ のりえ)
- 京都府立医科大学 大学院医学研究科 地域保健医療疫学
- 講師
- 小山 晃英(こやま てるひで)
- 九州大学医学研究院 連携総合診療内科学
- 准教授
- 池崎 裕昭(いけざき ひろあき)
- 近畿大学医学部 大学院医学研究科 公衆衛生学
- 滋賀医科大学 社会医学講座
- 准教授
- 高嶋 直敬(たかしま なおゆき)
- 佐賀大学 医学部医学科 社会医学講座
- 教授
- 田中 恵太郎(たなか けいたろう)
- 徳島大学大学院 医科学教育部・医学研究科 社会環境医学講座 予防医学分野
- 教授
- 有澤 孝吉(ありさわ こうきち)
- 静岡県立大学 品栄養科学部栄養生命科学科 公衆衛生学研究室
- 教授
- 栗木 清典(くりき きよのり)
- 広島大学大学院 医学系研究科 口腔保健疫学
- 名古屋大学大学院 医学系研究科 予防医学
- 教授
- 内藤 真理子(ないとう まりこ)
- 名古屋大学大学院 医学系研究科 予防医学
- 教授
- 若井 建志(わかい けんじ)
- 大阪大学大学院 医学系研究科 循環器内科学
- 教授
- 坂田 泰史(さかた やすし)
- 招聘教員
- 砂 真一郎(すな しんいちろう)
- 東北大学大学院 循環器内科学
- 准教授
- 坂田 泰彦(さかた やすひこ)
- 大阪府立病院機構 大阪国際がんセンター
- 名誉総長
- 堀 正二(ほり まさつぐ)
- 開西学院大学 人間福祉学部・人間福祉研究科
- 教授
- 佐藤 洋(さとう ひろし)
関連タグ

