死細胞の核からDNAを抽出し、免疫応答を惹起
―ヌクレオサイトーシスの発見―
- プレスリリース
2026年2月19日
東京大学
発表のポイント
- 免疫細胞が死んだ細胞の核からDNAを抽出して免疫応答を惹起する現象を発見し、「ヌクレオサイトーシス」と名付け、その誘導機構を解明しました。
- ヌクレオサイトーシスを誘導するヒドロキシクロロキン等の物質を同定しました。
- LCI-S等により、ヌクレオサイトーシスやIFN-β産生の可視化に成功しました。
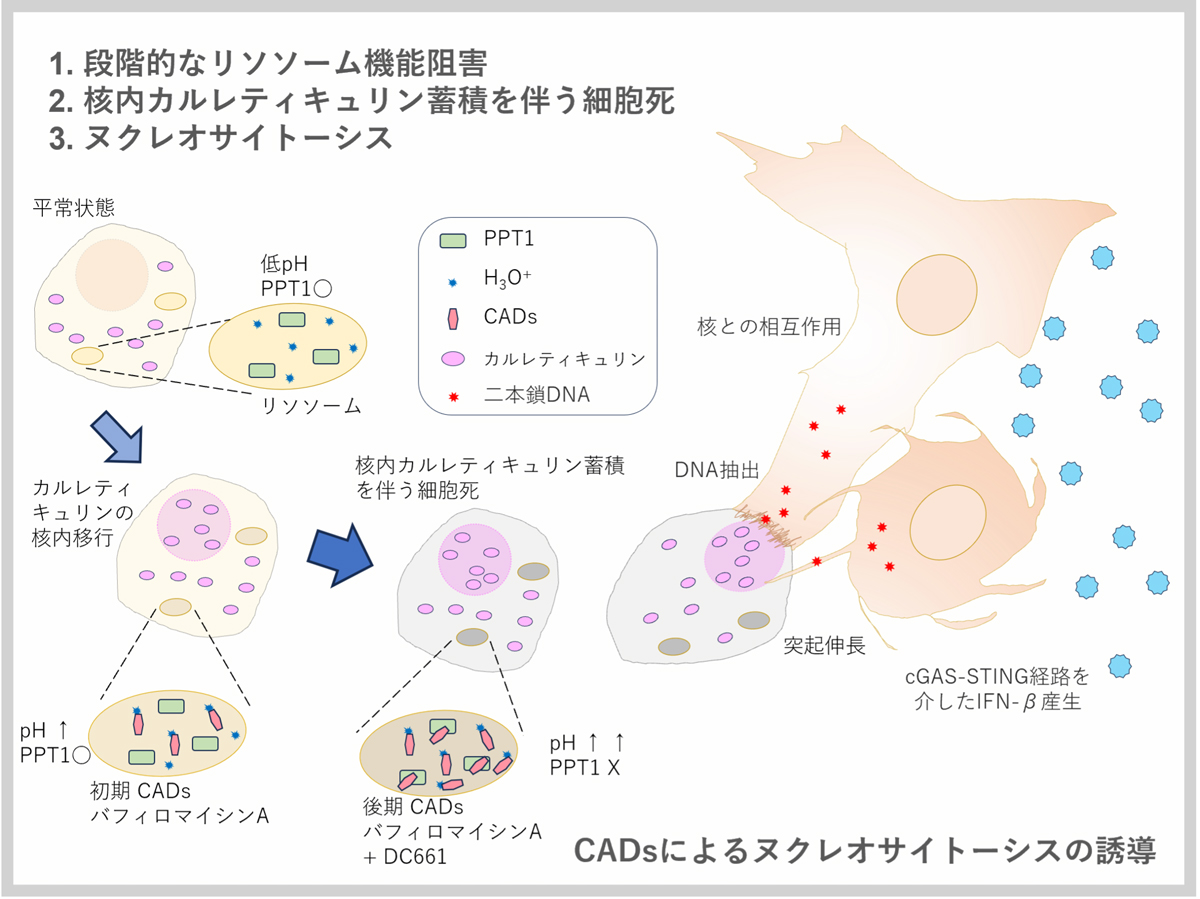
概要
東京大学医科学研究所ワクチン科学分野の石井健教授、同大学定量生命科学研究所免疫・感染制御研究分野の根岸英雄特任講師(研究当時:同大学医科学研究所ワクチン科学分野)、同大学大学院新領域創成科学研究科メディカル情報生命専攻の和田雄佑大学院生(研究当時)、及び同大学先端科学技術研究センターの白崎善隆准教授を中心とする研究者らは、免疫細胞が死細胞の核内DNAを抽出し、cGAS-STING(注1,2)経路を介して、I型インターフェロン(IFN-I:注3)産生をはじめとする免疫細胞の活性化を強力に誘導することを発見し、「ヌクレオサイトーシス」(注4)と名付けました。
ヒドロキシクロロキン(HCQ:注5)をはじめ、HCQと共通の構造的特徴を有するカチオン性両親媒性薬剤(CADs:注6)によって引き起こされる本現象は、感染症、がん及び自己免疫疾患などへの病態解明や治療戦略に関わる重要な情報を提供し、cGAS-STING経路が関与する疾病の薬剤開発基盤となることが期待されます。
本研究成果は2026年2月18日(英国標準時間)付で、英国科学雑誌「Nature Communications」(オンライン版)に掲載されました。
発表内容
死細胞などに由来する自己DNAは、細胞質内のcGAS-STING経路を介したIFN-I産生を誘導し、免疫応答を活性化することで、さまざまな疾患に関与することが知られています。しかしながら、自己DNAがどのようにして細胞の内部に存在するcGAS-STING経路を活性化するかは十分に明らかになっていませんでした。本研究では、免疫細胞が死細胞から核内DNAを抽出し、細胞質まで取り込むことでcGAS-STING経路を介してIFN-Iの産生をはじめとした免疫細胞の活性化を引き起こす現象を発見し、「ヌクレオサイトーシス」と名付けました。また、ヌクレオサイトーシスを誘導するための細胞死には、リソソーム内pH上昇及びパルミトイルタンパク質チオエステラーゼ1(PPT1:Palmitoyl-Protein Thioesterase 1:注7)の阻害による重度のリソソーム機能不全が必要であることを明らかにしました。さらに、HCQをはじめ、共通の立体構造を持ったCADsには、特殊な細胞死の誘導によって、ヌクレオサイトーシスを活性化する作用があることを明らかにしました。
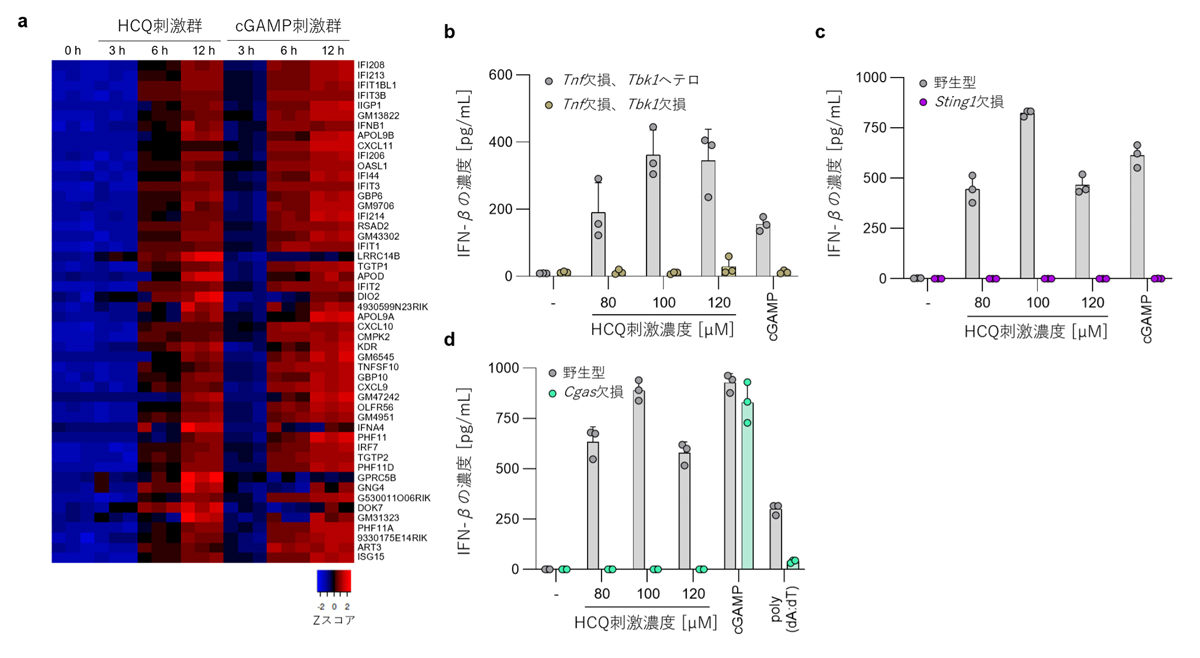
まず、研究者らは新型コロナウイルス(SARS-CoV-2)のパンデミックにおいて治療薬候補として抗ウイルス活性が報告された化合物やそれらに関連する化合物の中から、IFN-I誘導活性のある化合物を同定しました。その代表的な化合物の一つはHCQであり、顆粒球-マクロファージ刺激因子(GM-CSF:Granulocyte-Macrophage Colony-Stimulating Factor)存在下で培養したマウス骨髄細胞(GM-BMCs:GM-CSF-treated Bone Marrow-derived Cells)をHCQで処理をすると、代表的な抗ウイルス性サイトカインであるインターフェロンβ(IFN-β:Interferon-Beta)をはじめとする、さまざまな免疫応答関連遺伝子の発現誘導が確認されました(図1a)。興味深いことに、このHCQによる遺伝子発現誘導は、IFN-Iの強力な誘導因子であるSTINGのリガンド、環状GMP-AMP(cGAMP:cyclic GMP-AMP)による誘導と同レベルでした。また、このIFN-β誘導はタンパク質レベルでも産生が確認され、cGAS、STING、TBK1(注8)欠損細胞では完全に消失したことから、cGAMPによる古典的な誘導と同様の経路を介していることが示唆されました(図1b-d)。これら結果はHCQのみならず、アモジアキン(注9)、チロロン(注10)といった他の化合物においても確認され、これらは立体構造に共通性を持つことも判明しました。
次に研究者らは、HCQによるIFN-β産生の機構を解析するため、HCQ処理したGM-BMCsをさまざまな顕微鏡を用いて観察しました。その結果、生細胞から近接した核酸染色陽性死細胞の核に向けて突起を伸ばしている様子が観察されました(図2a)。同様の結果はホログラフィック顕微鏡(注11)による観察でも得られ、さらにその突起内の核酸も確認されました(図2b)。また、FACSDiscover S8セルソーターを用いたイメージサイトメトリー解析では、HCQ処理後に、生細胞と死細胞の境界面において、核酸染色による蛍光強度が有意に増加していました(図2c)。最後に1細胞分泌実時間イメージング顕微鏡法(LCI-S:Live-Cell Imaging of Secretion activity:注12)により、細胞間相互作用を可視化したところ、核酸移動後にIFN-β産生が確認されました(図2d)。一連の突起伸長による近接細胞からのDNA抽出、それに引き続くcGAS-STING経路の活性化と免疫応答の惹起という現象を研究者らは「ヌクレオサイトーシス」と名付けました。

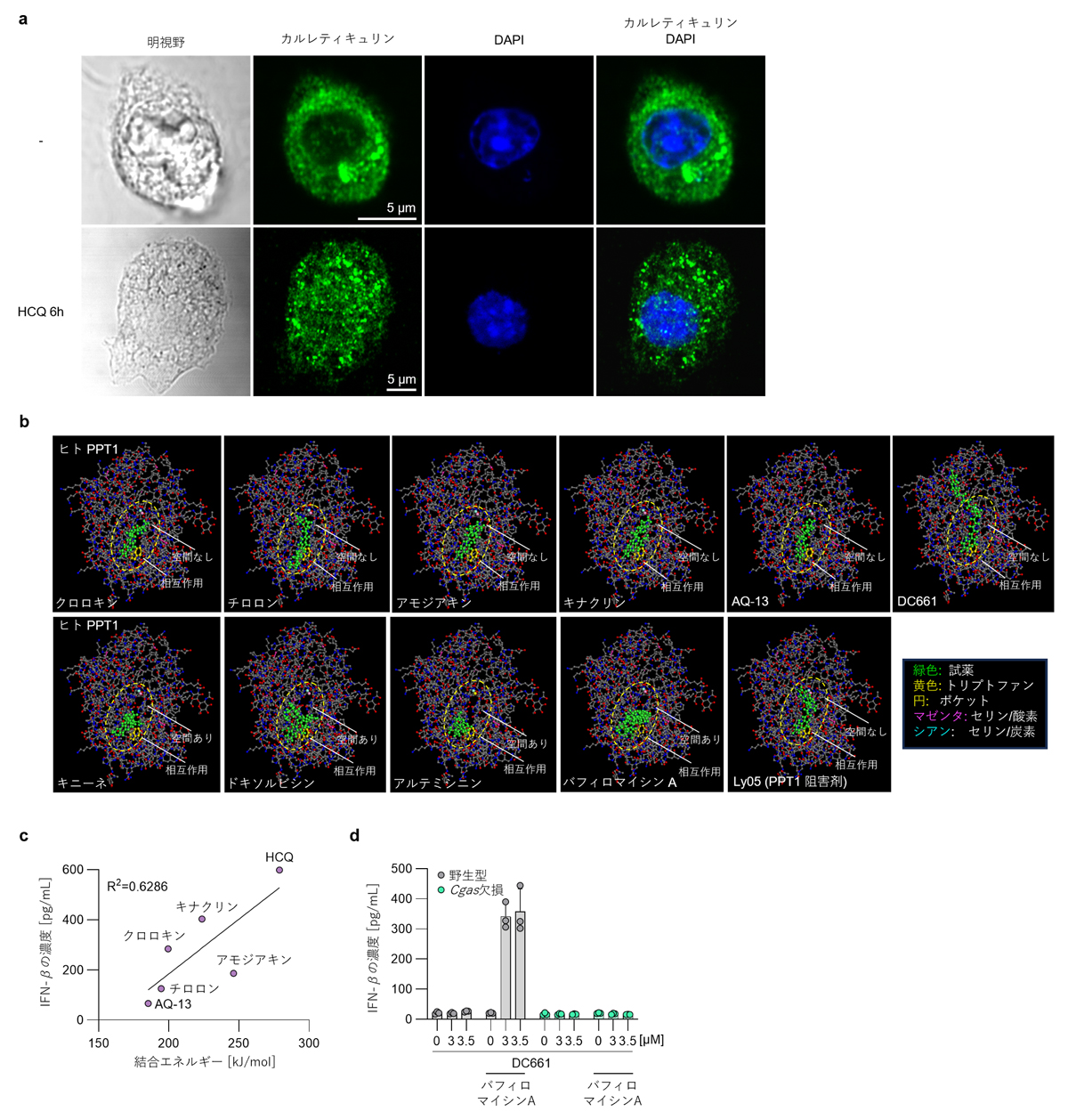
死細胞への突起の伸長を誘導する機構について研究者らは、腫瘍細胞の細胞死におけるeat-meシグナル(注13)として知られているカルレティキュリン(注14)に着目しました。HCQ処理細胞のカルレティキュリンの局在を確認したところ、カルレティキュリンのシグナルがDNA陽性領域である核で確認され、HCQ処理によるカルレティキュリンの核内蓄積が示唆されました(図3a)。この結果は、核に免疫細胞を呼び寄せるタンパク質の蓄積が起こっていることを示しています。
さらに、スーパーコンピュータを用いた構造シミュレーションの結果から、IFN誘導性CADsはPPT1に結合すること(図3b)、中性域におけるPPT1への結合活性とCADsのIFN-β産生との間に相関があること(図3c)、PPT1阻害剤(DC661)は非常に弱いIFN-β誘導活性であるが、リソソーム阻害剤であるバフィロマイシンAとの組みあわせによってcGAS依存的な強いIFN-β産生が誘導されること(図3d)が明らかとなりました。これらの結果より、ヌクレオサイトーシスの惹起には、IFN誘導性CADsによるリソソームpH上昇及びPPT1の阻害によるリソソーム機能不全が必要であることが示唆されます。
発表者・研究者等情報
東京大学
医科学研究所
感染・免疫部門 ワクチン科学分野
石井 健 教授
兼 同研究所 国際ワクチンデザインセンター
兼 同大学国際高等研究所 新世代感染症センター(UTOPIA)
小檜山 康司 准教授(研究当時)
Burcu Temizoz 助教
林 智哉 助教
黒澤 弥那 学術専門職員(研究当時)
松田 優々月 研究実習生
小島 大知 研究実習生
感染・免疫部門 マラリア免疫学分野
Cevayir Coban 教授
基礎医科学部門 分子シグナル制御分野
武川 睦寛 教授
久保田 裕二 講師
基礎医科学部門 RNA制御学分野
稲田 利文 教授
鈴木 亨 助教
附属幹細胞治療研究センター 幹細胞分子医学分野
岩間 厚志 教授
定量生命科学研究所
応用定量生命科学研究部門 免疫・感染制御研究分野
根岸 英雄 特任講師(研究当時:同大学医科学研究所 感染・免疫部門 ワクチン科学分野)
大学院新領域創成科学研究科
メディカル情報生命専攻
和田 雄佑 修士課程(研究当時)
アイリッシュ 彰音 ロード 修士課程
先端科学技術研究センター
光量子イメージング分野
白崎 善隆 准教授
大学院理学系研究科
生物科学専攻 生物化学講座 分子炎症免疫学研究室
反町 典子 教授
横浜市立大学
大学院医学研究科 免疫学
田村 智彦 教授
藩 龍馬 講師
千葉県がんセンター研究所
進化腫瘍学研究室
末永 雄介 室長
武藤 大将 研修生(千葉大学大学院 医学薬学府 博士課程)
兵庫医科大学
医学部 免疫学講座
黒田 悦史 主任教授
医学部 遺伝学
大村谷 昌樹 主任教授
理化学研究所
環境資源科学研究センター 触媒・融合研究グループ
闐闐 孝介 専任研究員
国立病院機構九州医療センター
感染症内科
長崎 洋司 科長
株式会社ライブセルダイアグノシス
山岸 舞 代表取締役
株式会社日立製作所
研究開発グループ
岩崎 富生
株式会社理論創薬研究所
吉森 篤史 代表取締役社長
株式会社インテージヘルスケア
金井 千里
論文情報
- 雑誌名:
- Nature Communications
- 題 名:
- cGAS-IFN-I responses by extracting nuclear DNA from dying cells via nucleocytosis
- 著者名:
- Hideo Negishi#,*, Yusuke Wada#, Yoshitaka Shirasaki#, Tomoya Hayashi, Yuji Kubota, Tomio Iwasaki, Mina Kurosawa, Tatsuma Ban, Daisuke Muto, Yusuke Suenaga, Taichi Kojima, Yuzuki Matsuda, Sean Lord Irish, Kosuke Dodo, Toru Suzuki, Mai Yamagishi, Burcu Temizoz, Atsushi Yoshimori, Chisato Kanai, Yoji Nagasaki, Masaki Ohmuraya, Tomohiko Tamura, Atsushi Iwama, Toshifumi Inada, Etsushi Kuroda, Kouji Kobiyama, Noriko Toyama-Sorimachi, Mutsuhiro Takekawa, Cevayir Coban, Ken J. Ishii*
#:共同筆頭著者、*:責任著者 - DOI:
- 10.1038/s41467-026-68839-w
- URL:
- https://www.nature.com/articles/s41467-026-68839-w
研究助成
本研究は、日本医療研究開発機構(AMED)「難治性疾患実用化研究事業(内在性炎症性RNA分子による全身性エリテマトーデスの病態発症・増悪機構の解明とその機構を標的とした治療法の確立)」、先進的研究開発戦略センター(SCARDA)「ワクチン開発のための世界トップレベル研究開発拠点の形成事業(UTOPIA)」、「ワクチン・新規モダリティ研究開発事業(100日でワクチンを提供可能にする革新的ワクチン評価システムの構築)(革新的アジュバント・ワクチンキャリアの開発と技術支援ならびにデータベースの構築)」、日本学術振興会 科学研究費助成事業(JP18K08406、JP21H02961)、科学技術振興機構 戦略的創造研究推進事業(JPMJCR18H1)などの支援によって行われました。
用語解説
- (注1)cGAS(cyclic GMP-AMP synthase)
細胞質でDNAを認識し、STINGのリガンドを合成するタンパク質。 - (注2)STING(stimulator of interferon genes)
インターフェロン遺伝子刺激因子。cGASとともに、細胞質DNAに対して免疫を活性化するタンパク質。 - (注3)I型インターフェロン(IFN-I:type I interferon)
抗ウイルス活性を有する最も典型的なタンパク質の一つ。 - (注4)ヌクレオサイトーシス
免疫細胞が死細胞の核からDNAを抜き取る新しい現象。 - (注5)ヒドロキシクロロキン(HCQ:hydroxychloroquine)
抗マラリア活性などを持つ低分子化合物。 - (注6)カチオン性両親媒性薬剤(CADs:cationic amphiphilic drugs)
カチオン性両親媒性薬剤。水溶性と脂溶性の両方の性質を有する。 - (注7)パルミトイルタンパク質チオエステラーゼ1(PPT1:Palmitoyl-Protein Thioesterase 1)
リソソーム中の酵素。タンパク質の分解や局在の制御に関与する。 - (注8)TBK1:TANK-binding kinase 1
I型IFNの産生に関与するキナーゼ。 - (注9)アモジアキン
抗ウイルス作用や抗マラリア活性を有する低分子化合物。 - (注10)チロロン
抗ウイルス作用を有する低分子化合物。 - (注11)ホログラフィック顕微鏡
細胞や細胞小器官をリアルタイムかつ無染色で可視化する技術。 - (注12)LCI-S:Live-Cell Imaging of Secretion activity
生細胞から分泌されるサイトカインをリアルタイムで可視化する技術。 - (注13)eat me シグナル
死細胞の表面に発現し、マクロファージ等による取り込みを促進するタンパク質。 - (注14)カルレティキュリン
eat me シグナルとして知られるタンパク質の一つ。特定の細胞死の際、細胞表面に移行する。
問合せ先
東京大学先端科学技術研究センター 光量子イメージング分野
准教授 白崎 善隆(しらさき よしたか)
関連タグ

