- ホーム
- 研究について
- 研究者紹介 フロントランナー
- 004:大澤 毅 特任准教授
004:大澤 毅 特任准教授
大澤 毅 特任准教授

大澤 毅 特任准教授
ニュートリオミクス・腫瘍学 分野
公開日:2019年 8月 6日
がん細胞の生態を、栄養の視点から解き明かす
「ニュートリオミクス」が切り拓く、がん研究の未来
がん細胞も「生きて」いる。それには栄養や酸素が必要だ。ならば、その供給を遮断すれば、がん細胞の増殖を止められるはずだ。だが、話はそう単純ではない。むしろ、低栄養や低酸素の過酷環境で、がん細胞も生き延びるために環境に適応する。その結果、転移能や浸潤能、薬剤耐性を獲得し、がん細胞は「悪性化」する。 ニュートリオミクス・腫瘍学分野の大澤毅特任准教授は、がん細胞の生態を、栄養の視点も交えて解析する研究に取り組む。がん細胞の生態解析に使うのが、ゲノムやエピゲノム(DNA)、トランスクリプトーム(RNA)、プロテオーム(タンパク質)、メタボローム(代謝産物)といった多階層のオミクス解析だ。それに栄養(ニュートリション)の視点を取り込んだのが「ニュートリオミクス」である。この新たなアプローチで、がん細胞が過酷環境で生き延びるメカニズムの解明に挑む。
過酷な環境で、がん細胞は隠れて生き延びる
体内の細胞は、血管を介して栄養や酸素を受け取っている。それはがん細胞も同様だ。がん細胞が増殖する際、栄養を採るために血管が多くつくられるが、これを「血管新生」と呼ぶ。そこに着目したのが、「血管新生阻害療法」だ。血管新生を阻害して栄養や酸素を遮断する。すなわち“兵糧攻め”により、がん細胞の増殖阻止を狙う治療法である。大澤特任准教授がかつて東京大学医科学研究所に所属していた際(2006年1月~2007年4月)、師事した澁谷正史教授は、がん細胞における血管生物学研究の第一人者だった。
ところがこの治療法は、ある程度有効ではあるものの、あまり効かないケースもあった。それだけではない。転移能や浸潤能、抗がん剤への耐性を獲得するがん細胞が見られた。その理由を探っていくなかで考えついたのが、「栄養や酸素が十分に行き届かない環境で、がん細胞は悪性化する」という仮説だった。
「この仮説を検証するため、通常の培地で培養したがん細胞と、栄養素を抜いた培地と酸素や栄養が少ない環境で育てたがん細胞を、それぞれマウスに移植する実験を行いました。結果は仮説どおりで、低栄養・低酸素の環境で生き残ったがん細胞は、転移能が明らかに高まっていました」(図1参照)
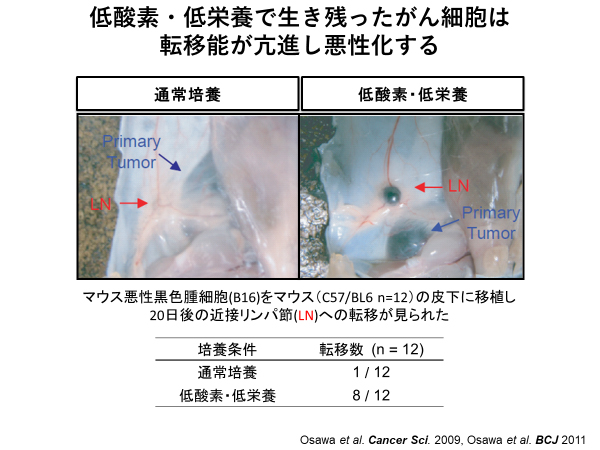
以来一貫して、大澤特任准教授は、がん細胞と栄養に関する研究に取り組んでいる。そのアプローチを、「ニュートリオミクス」と名付けた。「栄養」を意味する「ニュートリション」と、オミクス解析を組み合わせた造語だ。
オミクス解析とは、ゲノムやエピゲノム(DNA)、トランスクリプトーム(RNA)、プロテオーム(タンパク質)、メタボローム(代謝産物)などの生体分子を網羅的に解析する技術で、近年、これら多階層のオミクス解析を統合する研究が盛んに行われ、生体内での分子の働きが次々と明らかにされている。大澤特任准教授は、この統合オミクス解析と栄養の視点を組み合わせ、がん細胞が過酷環境でどのように生き延びるのかという解明とともに、新たながん治療法の確立を目指している。
栄養素の欠乏に、がん細胞はどう適応するのか
大澤特任准教授は、次の3項目を研究の柱として掲げている。いずれも独立する研究ではなく、それぞれ密接に関わり合うものだ。
- (1)新しいオンコメタボライト(がん代謝産物)を同定する。
- (2)糖質・脂質・アミノ酸⽋乏におけるがん適応機構を明らかにする。
- (3)新しい栄養学「ニュートリオミクス」の視点からがんの治療法を開発する。
(1)の「オンコメタボライト」とは、がん細胞の増殖や生存に寄与する代謝産物のことだ。大澤特任准教授は、特に低栄養・低酸素下における新たなオンコメタボライトの発見に力を入れている。その結果、新たなオンコメタボライトの同定に成功しつつある。
発見したのは、がん細胞の中に溜まってくる飢餓応答性のがん代謝物である。この物質は、細胞膜を構成する要素のひとつ、すなわち細胞膜を合成する過程の中間代謝物だ。
「このがん代謝物を低栄養のがん細胞に与えると、がん細胞が生き延びやすくなります。がん細胞がそれを餌代わりにしているのか、この物質の蓄積が何らかの代謝経路のスイッチを入れるのか、そこはまだよく分かっていませんが、その仕組みの解明をいま進めているところです」と大澤特任准教授。

そもそも、低栄養のがん細胞では、どのようにしてこのがん代謝物が溜まっていくのだろうか。
「低栄養のがん細胞は、増殖速度が緩やかになります。それにあわせて細胞膜の合成も途中で止まります。その結果、中間代謝物が溜まってくるわけです」
さらに大澤特任准教授らは、低栄養下で細胞膜合成経路が止まるメカニズムも明らかにした。たったひとつのアミノ酸の欠乏が、細胞膜合成経路のスイッチをオフにしていたのだ。
「スイッチの働きをしているのはアミノ酸です。低栄養のがん細胞でアミノ酸が欠乏すると、細胞膜合成経路が止まり、細胞膜合成経路の中間代謝物ががん細胞の中に溜まってきます。それが、何らかのメカニズムでがん細胞を生き延びやすくしているのです」
このように、たったひとつの栄養素の欠乏が、がん細胞の代謝を大きく変えることがある。低栄養下で、がん細胞はどのように生き延びているのか。それを明らかにするのが上記の(2)の研究だ。
「糖がなくなるとがん細胞の代謝はどう変わるのか。それがアミノ酸なら、あるいは脂質ならどうなるか。それを栄養素ごとにひとつずつ調べています。アミノ酸が欠乏したら飢餓応答性のがん代謝物が溜まり、それががん細胞の代謝を変えるように、脂質が欠乏したら、がん細胞は酢酸を栄養素にして生き延びることが明らかになりました。ここから分かるのは、ひとつの栄養素が欠乏しても、代替の代謝経路が作動して、がん細胞は生き延びられる可能性が高いということです。ならば、複数の栄養素が欠乏したらどうなるか。合わせ技による治療効果についても研究を進めています」
従来の常識を超える、ある画期的な発見
低栄養・低酸素環境下におけるがん細胞代謝を調べる過程で、大澤特任准教授らは、ある画期的な発見もしている。それと関連するのが、1956年にドイツの生理学者オット・ワーバーグ博士が提唱した、『がん細胞は酸素を使わず、嫌気的解糖系を利用して生き残る』という「ワーバーグ(ワーブルグとも)効果」だ。
嫌気的解糖系、すなわち嫌気呼吸は、酸素を使う好気呼吸と比べてきわめて効率が悪い。好気呼吸では、グルコース1分子あたり細胞のエネルギーとなるATPが38分子生成されるが、嫌気呼吸では4分子しか生成されない。「がん患者が痩せていくのは、ATP産生のために糖質が多く使われるからかもしれない」と大澤特任准教授は説明する。 この「ワーバーグ効果」によって、がん細胞の周辺のpHが下がり、酸性に傾くことが知られていた。嫌気的解糖系によって細胞内に乳酸やプロトン(陽子)が溜まり、それが細胞外に排出され、細胞周辺のpHが低くなるのだ(図2参照)。
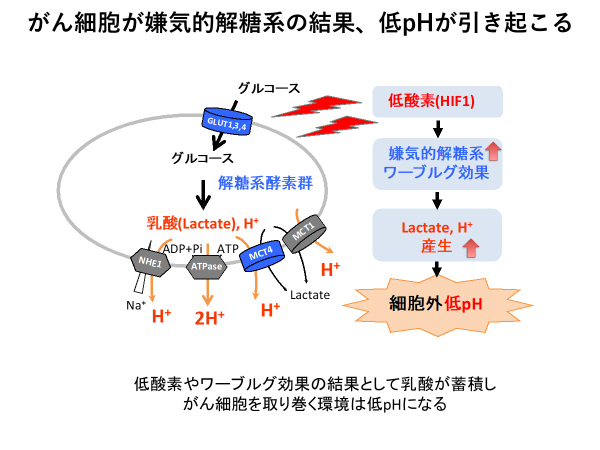
「細胞外の低pHは、ワーバーグ効果による結果だと考えられていましたが、酸性状態ががん細胞にどのような影響を及ぼすかは解明されていませんでした。最近の研究で、酸性環境ががんの悪性化を促進している可能性が指摘されていることに私たちも注目し、酸性環境にがん細胞がどのように応答しているかを詳しく調べてみました」
研究によって見えてきたのは、あるタンパク質の働きだ。細胞内でコレステロール代謝のスイッチをオン・オフする転写制御因子が、酸性環境のがん細胞で活性化する。その結果、がん細胞内でコレステロールや酢酸を代謝する酵素群の遺伝子発現も活発になり、がんの増殖や患者の予後悪化に寄与することを確認したのだ。
「酸性環境で特異的に働く代謝経路を阻害することができれば、がん細胞の増殖を抑えることができます」と大澤特任准教授。薬剤開発に向けた研究も進行中とのことだ。
創造性を育む空間を意識した研究室
大澤特任准教授が研究者を志したいきさつにも触れておきたい。祖父の代から続く建設会社の家に生まれた。子どもの頃から漠然と、会社を継ぐものと考えていたが、父から「小さな世界で生きるのではなく、未来が開けることに挑戦しろ」と言われたのをきっかけに、英国・ロンドン大学への留学を決めた。
そしてこの選択が、がん研究者への道につながっていく。ロンドンで師事した教授陣が優れたがんの研究者であったことに加え、近親者にがんを発症した人が多かった。特に、留学先で博士課程に入学したその日に祖母をがんで亡くしたことは、がん研究への思いを強くする出来事になった。
がんのメカニズム解明や治療法開発を巡っては、世界中の研究者がしのぎを削って研究に取り組んでいる。こうした激しい競争環境で研究を続けることを、大澤特任准教授はどう見ているのだろうか。
「がん全体で広く見れば、競争が激しいのはたしかです。ただ、栄養の観点からがん細胞の代謝の研究に取り組んでいる人はそう多くはありません。私は私たちにしかできない独自の研究をしたいと思います。どんな研究でもそうでしょうが、少し視点を変えれば自分たちのオリジナリティを発揮できるはずです」

「他人の論文はほとんど読みません。読めばバイアスがかかり、研究がその方向に寄ってしまうからです。とはいえ、研究のトレンドを押さえておくことも重要です。そのため学会や研究会には積極的に参加し、誰がどのような研究をしていて、どんな方向に進もうとしているのかを把握しています」
独自性へのこだわりは、研究内容だけではなく研究環境にも溢れている。研究室には、実験を行うラボと、実験で得られたデータを解析したり、論文を読んだりするための居室の2つのエリアがある。木のぬくもりと白を基調とした居室は、大きな窓から生い茂る樹木を望め、明るい陽射しが射し込む。隣のラボはガラス張りで、大学内の研究室とは思えない明るくオープンな雰囲気だ。
「居室をカフェやオープンスペースのように、ゆっくりリラックスしてものを考えられるような空間にすることを意識しました。私が学生の頃は狭くて暗い居室を使っていましたが、そんな空間で考えているとすぐに煮詰まってしまい、よく研究室から逃げ出してカフェやオープンスペースに行ったものです。リラックスできる空間のなかでこそ、自由なアイデアや創造性に溢れた発想が生まれてくる。そのための空間をデザインできたと思っています」

ソフト面での取り組みも特筆しておきたい。研究室には大学院生を含め10名ほどが在籍しているが、そのうち一人はアートデザイナーだ。大澤特任准教授はその理由を次のように語る。
「研究成果をより分かりやすく伝えるためです。細胞内の複雑な動きを言葉だけで説明するのは難しく、図やイラストにするにも、自分が描くとどうしても素人の絵になってしまいます。すでに、海外の研究室では3D画像やCG、動画を使ったプレゼンが当たり前になってきています。今後は、CGやムービーなどの映像を用いて研究成果を説明する検討も始めています」
研究を大きく前に進める、研究所内での異分野融合
先端研では、ユニークで優れた人材の獲得を目的に、若手研究室主催者を「特任制度」によって採用している。この制度のもとで着任した一人が大澤毅特任准教授だ。
加えて、2018年度からは生命・情報科学分野において突出した若手研究者が交流し、協業して最先端の研究に挑むプロジェクトをスタートさせた。それが「東京大学生命・情報科学若手アライアンス(UTokyo-RAILS)」だ。若手研究室主催者のラボ間の壁を取り払い、大規模先端装置の共有やコミュニティ機能を発揮できるオープンラボラトリーも整備した。大澤特任准教授は、そのメンバーの一人でもある。
UTokyo-RAILSには、分子生物学や計測科学、データサイエンスやAIなど多分野の若手研究者が集まり、生命科学の大きな課題に挑んでいる。生命科学はウェット(実験)とドライ(情報)の両輪が欠かせない総合科学になっているなか、大澤研究室は主にウェットに注力している。アライアンスのなかに、ドライの情報解析に長けたラボがあり、連携して研究を進めている。

「同じ研究所内、しかも物理的に同じ建物内のすぐ近くに、研究室どうし助け合える環境がある。そのおかげで、研究がとてもスムーズに進んでいます。私たちが実験で得たデータをすぐ解析してもらうことができますし、解析結果の情報共有もきわめてスムーズです。互いに頻繁に研究室を行き来しあい、非常に密度の濃いシナジーが生まれていると感じています」
オープンな研究室で生まれたアイデアが、異分野との密な連携を通じて磨きがかかる。この環境が、ニュートリオミクスという独自のアプローチのがん研究を、大きく前に進めていくことになるのだろう。

2001年に英国ロンドン大学キングスカレッジ生化学部卒業。1999年6月~8月、米国ハーバード大学物理学留学。2005年12月英国ロンドン大学がん研究所(UCL)大学院腫瘍学専攻、博士課程修了、腫瘍学博士(2010年取得)。2000年6月~7月、英国ロンドン大学 キングスカレッジ生化学教室技術補佐員。同年7月~8月、国立循環器病センター研究所 病因病理部 インターンシップ。2006年 東京大学医科学研究所腫瘍抑制分野研究員。2007年 東京大学医科学研究所システム生命科学リサーチフェロー、東京医科歯科大学分子腫瘍医学分野 特任助教。2011年 東京大学先端科学技術研究センターシステム生物医学分野特任助教、2018年より現職。
関連タグ

