酸性がん微小環境におけるがん細胞の生存戦略を解明
―酸性腫瘍微小環境で膵癌細胞は細胞死を回避し、補体経路の活性化を介した免疫調節が慢性的な酸性への耐性に関与する―
- プレスリリース
2026年4月17日
東京大学
発表のポイント
- 腫瘍微小環境における酸性環境下では、がん細胞や腫瘍は細胞死を回避していますが、その機構は不明な点が多いです。本研究では、酸性環境はがん細胞の腫瘍形成能と可塑性を強めていることを示しました。
- 慢性的な酸性培養系を用いて、これまで未知であった酸性環境における膵癌の細胞死の回避機構の解明に挑みました。その結果、酸性耐性に重要な遺伝子であるFAM129Cを同定し、さらに補体経路の活性化を介したがん悪性化メカニズムを明らかにしました。
- 本研究成果は酸性腫瘍微小環境に対して耐性を獲得した癌を標的とした新たな創薬の開発に繋がることが期待されます。
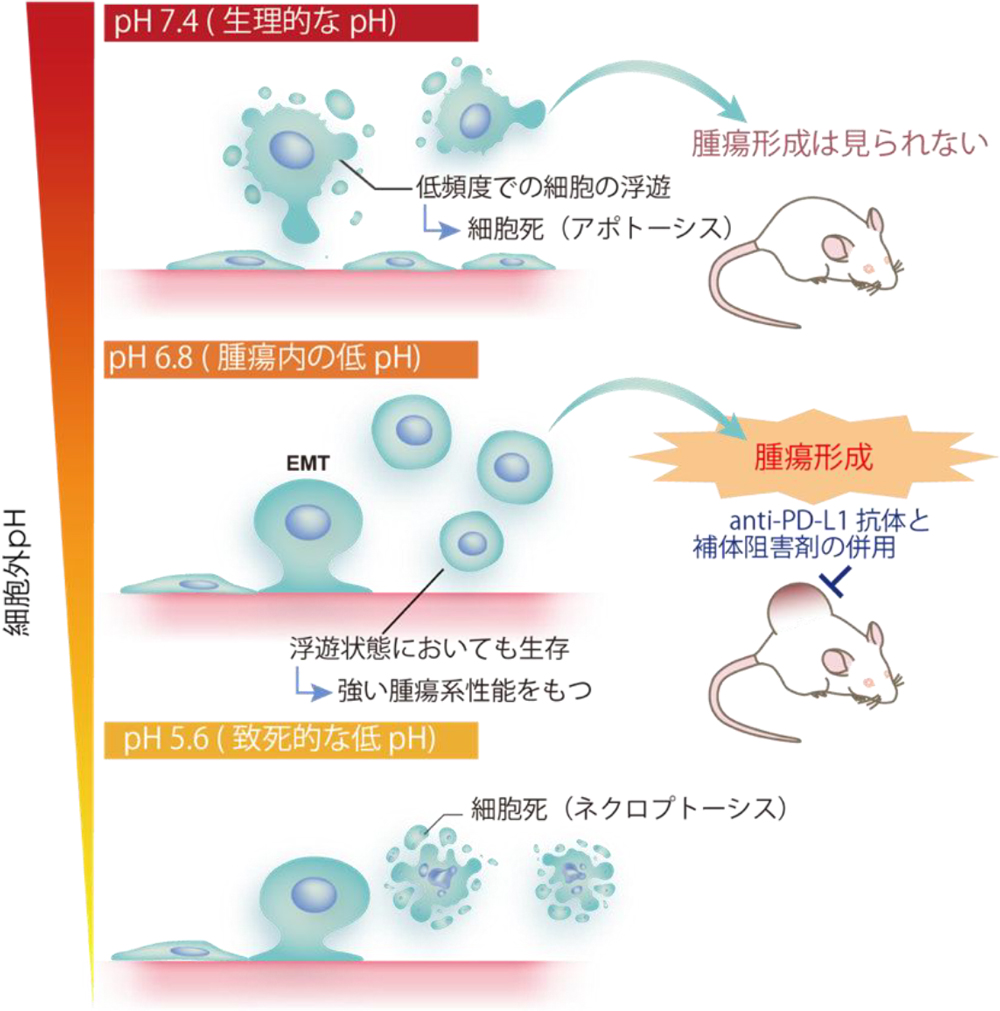
概要
東京大学先端科学技術研究センターの長谷川愛美学部学生(研究当時、現 大学院理学系研究科 修士学生)、徐博(ジョ・ハク)特任研究員、大澤毅准教授、柳井秀元特任准教授(研究当時、現 横浜市立大学 医学研究科 主任教授)、東京大学大学院工学系研究科の山東信介教授、ブリティッシュコロンビア大学(UBC)Biomedical Engineeringの谷内江望教授、北海道大学大学院情報科学研究院の松元慎吾教授、平田拓教授らによる研究グループは、酸性状態でのがん細胞の生存戦略の一端を解明しました。
固形がんでは血管構築不全による血流不足から、組織中心部が低酸素状態に陥りやすく、その代謝変容の結果として酸性状態(アシドーシス)になることが知られています。本研究では、酸性状態におけるがん細胞の新しい細胞死と生存メカニズムを解明しました(図1)。
これまで急性の酸性ストレス下での影響と比較して、慢性的な酸性環境下でのがん細胞の生存メカニズムについては十分に調べられてきませんでした。この研究成果は今後、酸性腫瘍微小環境に対して耐性を獲得した癌を標的とした新たな創薬の開発につながることが期待されます。
本研究成果は、2026年4月16日11時(米国東部夏時間)に国際科学誌「Cell Reports」に、オンライン掲載されました。
発表内容
がん細胞は好気的な環境下においても解糖系(注1)を亢進させる特徴的な代謝様式を示します。これはWarburg効果(注2)と呼ばれています。この結果、通常の組織ではpHが7.4ほどに保たれていますが、腫瘍付近のpHは6.0~6.8にまで下がります。これまで、我々の研究室では、この酸性腫瘍微小環境によって、コレステロールの生合成経路(文献1)やポリアミン経路の活性化(文献2)が起きることを報告してきました。しかしながら、がん細胞が酸性下でどのような生存戦略をとっているのかについては未解明でした。
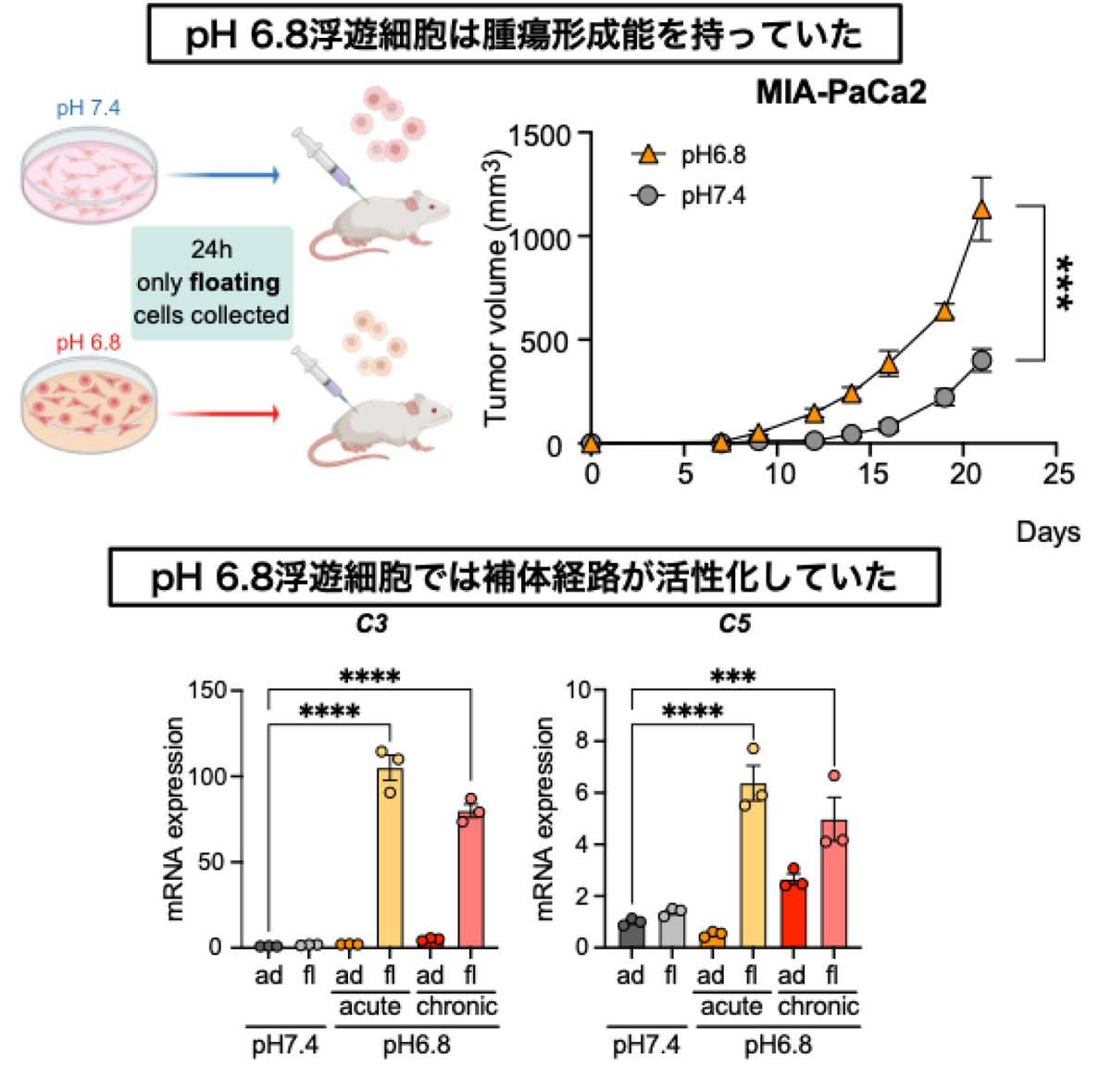
我々はまず様々な値のpH培養系を確立し、正常な組織(pH 7.4)および腫瘍組織(pH 5.6~6.8)を模倣した培養系を用意しました。まず、腫瘍中心部のpH(pH 5.6)ではネクロトーシス(注3)が引き起こされるものの、平均的な腫瘍のpH(pH 6.8)ではこの細胞死は回避されることを見出しました。さらに、pH 6.8の培養細胞で浮遊状態になる一部の細胞は足場非依存的に生存状態を保っており、腫瘍形成能も保持していることが明らかとなりました。このpH 6.8の浮遊細胞において活性化されている経路を調べるためにRNA-seqを行ったところ、pH 6.8の浮遊細胞では補体経路(注4)が活性化されていることが見出されました。さらに、慢性的な酸性培養環境において補体経路の遺伝子の発現が増強されました(図2)。
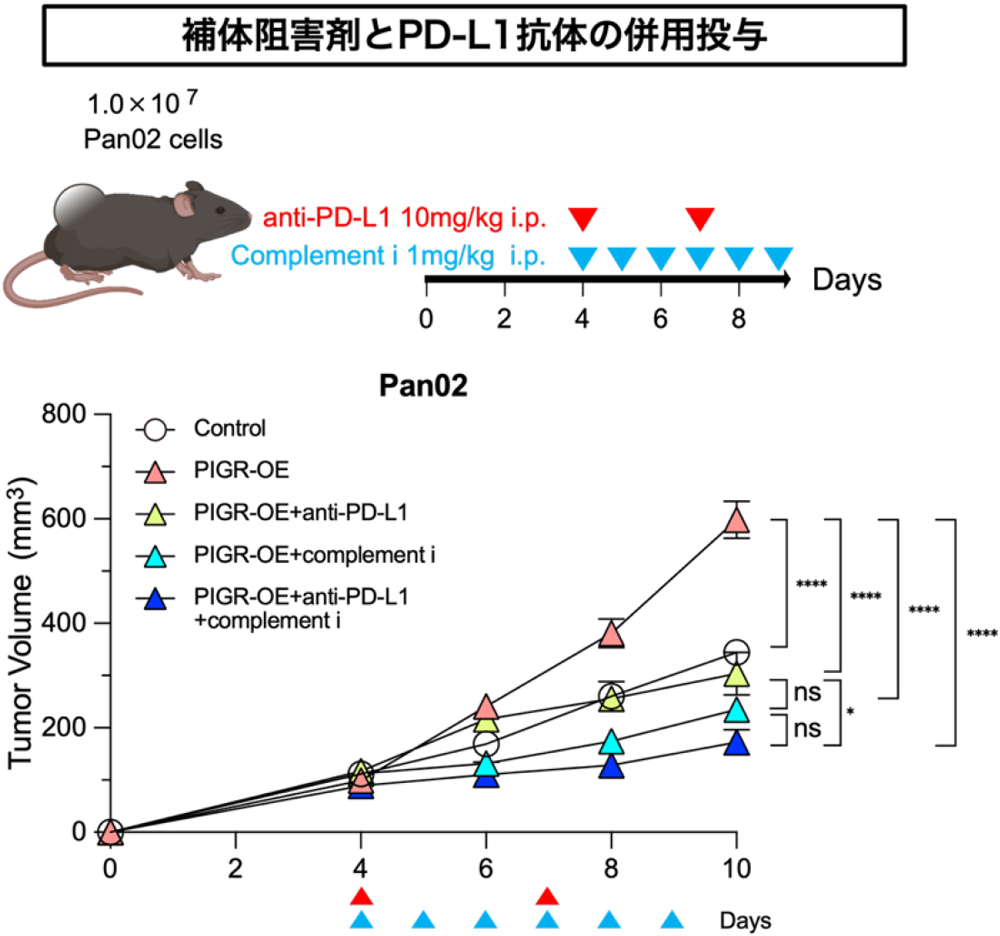
次に、この慢性的な酸性環境において酸性ストレス耐性への獲得に重要な遺伝子を解明するためCRISPRノックアウトスクリーニング(注5)とデータベース解析を行い、膵癌の予後不良と関わるFAM129Cを同定しました。さらに、FAM129Cの機能について検討するため、過剰発現細胞を作成したところ、多量体免疫グロブリン受容体のPIGRが最も抑制されていることを見出しました。このPIGRを過剰発現させると、マウスモデルで癌組織へのマクロファージの浸潤が促進されました。酸性耐性には補体経路が関わるという知見と合わせて、PIGRを過剰発現させた腫瘍に対してPD-L1抗体(注6)と補体経路の阻害剤を併用投与すると、相乗的にがん縮小効果を示しました(図3)。
本研究では、膵癌細胞が酸性下では細胞死を回避し、足場非依存的に生存状態や腫瘍形成能を維持し補体経路を活性化させていることを明らかにしました。また慢性的な酸性ストレスは、FAM129C-PIGRと補体経路を介してマクロファージの浸潤を促進させることを見出しました。近年、低酸素や低栄養以外に加えてがんの進展に関わる微小環境としてpHストレスが注目されています。またpHは生命活動に関わる指標であり、現在様々な研究グループが多種多様な生物でpHストレス応答メカニズムの解明に取り組んでいます。
本研究は、酸性腫瘍微小環境に対して耐性を獲得した癌を標的とした新たな創薬の開発や、生物が持つ本質的な酸性応答メカニズムの解明に繋がることが期待されます。
文献1:
Kondo, A., Yamamoto, S., Nakaki, R., Shimamura, T., Hamakubo, T., Sakai, J., Kodama, T., Yoshida, T., Aburatani, H., and Osawa, T. (2017). Extracellular Acidic pH Activates the Sterol Regulatory Element-Binding Protein 2 to Promote Tumor Progression. Cell Reports 18, 2228–2242.
https://doi.org/10.1016/j.celrep.2017.02.006.
文献2:
Kato, M., Maeda, K., Nakahara, R., Hirose, H., Kondo, A., Aki, S., Sugaya, M., Hibino, S., Nishida, M., Hasegawa, M., et al. (2023). Acidic extracellular pH drives accumulation of N1-acetylspermidine and recruitment of protumor neutrophils. PNAS Nexus 2, pgad306.
https://doi.org/10.1093/pnasnexus/pgad306.
発表者・研究者等情報
東京大学
先端科学技術研究センター ニュートリオミクス・腫瘍学分野
大澤 毅 准教授(兼:大学院工学系研究科、大学院理学系研究科)
長谷川 愛美 研究当時:工学部 学部学生
現:東京大学大学院理学系研究科 修士課程
徐 博 特任研究員
前田 啓介 研究当時:博士課程
蔡 菲菲 博士課程
崔 润美 修士課程
安藤 律子 学術専門職員
坂本 彩菜 学部学生(交流研究生)
ケイラ・ボイコット 日本学術振興会特別研究員PD
西田 美由紀 研究当時:学術専門職員
松本 健 協力研究員
岩渕 千里 特任研究員
安藝 翔 研究当時:特任助教
山形 一行 特任講師(兼:大学院工学系研究科)
土田 里香 協力研究員
先端科学技術研究センター 社会連携研究部門 炎症疾患制御分野
柳井 秀元 研究当時:特任准教授
現:横浜市立大学 医学研究科 主任教授
大学院工学系研究科
谷田部 浩行 助教
山東 信介 教授
ブリティッシュコロンビア大学
Biomedical Engineering
谷内江 望 教授
北海道大学
大学院情報科学研究院
松元 慎吾 教授
平田 拓 教授
福井大学
学術研究院 医学系部門 血管統御学分野
木戸屋 浩康 教授
川崎医科大学 生化学
栗林 太 教授
国立研究開発法人国立がん研究センター
研究所FIOC 薬効試験部門
高橋 真美 研究員
千葉大学 医学部附属病院がんゲノムセンター
関 元昭 特任助教
Max Delbrück Center for Molecular Medicine
中川 寿々花 博士課程
論文情報
- 雑誌名:
- 「Cell Reports」
- 題 名:
- Tolerance to extracellular acidic pH facilitates tumor plasticity
- 著者名:
- Manami Hasegawa, Bo Xu, Keisuke Maeda, Motoaki Seki, FeiFei Cai, Runmei Cui, Ritsuko Ando, Suzuka Nakagawa, Ayana Sakamoto, Cayla Boycott, Hiroyuki Yatabe, Miyuki Nishida, Ken Matsumoto, Chisato Iwabuchi-Yoshida, Sho Aki, Kazuyuki Yamagata, Rika Tsuchida, Mami Takahashi, Futoshi Kuribayashi, Hiroyasu Kidoya, Hiroshi Hirata, Shingo Matsumoto, Shinsuke Sando, Hideyuki Yanai, Nozomu Yachie and Tsuyoshi Osawa
- DOI :
- 10.1016/j.celrep.2026.117226
研究助成
本研究は、日本学術振興会(JSPS)科研費 新学術領域研究(20H04834)、学術変革領域研究A(25H01339、25A304)、基盤研究B、学術変革領域研究B(23H03861)、基盤研究C(24K10279)、挑戦的研究(萌芽)(19K22553、21K19399、23K18234)の助成、ならびに文部科学省 科研費 AdAMS(22H04922)、SGH財団、キヤノン財団、武田科学振興財団、高松宮妃癌研究基金、国立研究開発法人 科学技術振興機構(JST)創発的研究支援事業(JPMJFR2306)、国立研究開発法人日本医療研究開発機構(AMED)次世代がん医療創生研究事業(P-CREATE)「低pH がん微小環境のネットワーク撃滅を実現する標的分子群の同定と治療法の開発(JP17cm0106221)」、革新的がん医療実用化研究事業「がん微小環境の分子基盤に基づいた革新的がん治療薬の開発(JP19ck0106362)」の支援を受けて実施されました。
さらに本研究は、東京医科歯科大学 難治疾患研究所、金沢大学 がん進展制御研究所の共同研究拠点事業、および北海道大学 遺伝子病制御研究所の共同利用・共同研究拠点事業の一部支援も受けています。
用語解説
- (注1)解糖系
グルコースを燃料としミトコンドリア電子伝達系を介さずにエネルギーを産生する代謝経路である。増殖の速いがん細胞で亢進することが知られている。解糖系の亢進によりプロトンや乳酸が産生されるため、結果的にがん組織の内部が酸性状態に陥る。 - (注2)Warburg効果
好気的な環境下においても、がん細胞がミトコンドリア電子伝達系(OXPHOS)を介さず解糖系を優先し、ATPを産生するという現象。1920~1930年代にドイツの生化学者、Otto Warburg博士によって提唱された。 - (注3)ネクロトーシス
プログラムされた細胞死の1つ。RIP1、RIP3、MLKLが順次に活性化され、リン酸化MLKLが細胞膜上に重合体を形成し、細胞膜破裂が引き起こされて細胞死に至る。 - (注4)補体経路
血液や組織液中にある約30種類以上のタンパク質(補体)が連鎖的に活性化し、病原体の除去や炎症反応を促進する免疫システムのこと。本研究では酸性環境によって免疫細胞の動員に関わるC3やC5の発現が亢進していた。 - (注5)CRISPRノックアウトスクリーニング
CRISPR-Cas9システムを利用して全遺伝子をランダムにノックアウトして、様々な条件下で、生存した細胞や死滅した細胞を集めて解析する手法。本研究では、酸性ストレスへの耐性獲得に関与する遺伝子を同定するスクリーニング手法を行った。 - (注6)PD-L1抗体
免疫細胞(T細胞)上のPD-1とがん細胞上のPD-L1の結合を阻害し、T細胞ががん細胞を攻撃する能力を回復させる薬剤。現在、様々ながん治療に用いられている。
問合せ先
東京大学先端科学技術研究センター ニュートリオミクス・腫瘍学分野
准教授 大澤 毅(おおさわ つよし)
関連タグ

